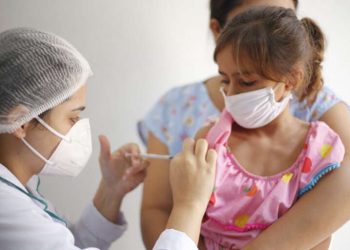
A Anvisa (Agência Nacional de Vigilância Sanitária) recebeu nesta sexta-feira (9) o pedido de registro definitivo da Coronavac pelo Instituto Butantan. Primeira vacina a ser aplicada no Brasil para iniciar a imunização dos brasileiros contra a covid-19, o imunizante está em uso emergencial desde 17 de janeiro do ano passado. O prazo para a análise do pedido é de 60 dias.
Curta e siga nossas redes sociais:
Sugira uma reportagem. Mande uma mensagem para o nosso WhatsApp.
Entre no canal do Revista Cariri no Telegram e veja as principais notícias do dia.
Segundo informou a Anvisa, a solicitação foi apresentada no âmbito de una resolução da agência que contém critérios e procedimentos extraordinários para pedidos de registro decorrentes do novo coronavírus.
A norma prevê, por exemplo, a análise prioritária e a possibilidade de se firmar termos de compromisso, como foi feito com outras vacinas contra a covid-19 já autorizadas no Brasil.
Como é o processo de análise
Com o pedido em mãos, a Anvisa vai fazer uma análise em três etapas, que, segundo a agência, é feita por três setores diferentes:
• a área de Medicamentos, que avalia os aspectos de segurança e eficácia;
• a área de Farmacovigilância, responsável pelo monitoramento e planos de acompanhamento da vacina após sua entrada em uso no país; e
• a área de Inspeção e Fiscalização, responsável pela avaliação das Boas Práticas de Fabricação.
Coronavac teve produção suspensa
No final do mês passado, o Butantan informou que a Coronavac teve sua produção suspensa. Segundo o instituto, a fabricação foi interrompida devido à falta de novos pedidos de lotes do imunizante.
No total, o Butantan —ligado ao governo paulista— disse que entregou mais de 110 milhões de doses ao Ministério da Saúde. O último envio ocorreu em fevereiro deste ano. Desde então, o intituto afirmou que não foi procurado para assinar novos contratos.
Em e-mail enviado, a assessoria do instituto disse que o Butantan tem “total capacidade de produção para atender a quaisquer demandas deste imunizante, à medida que sejam recebidas” e que não recebeu novas propostas do Ministério da Saúde para compra.
Fonte: UOL