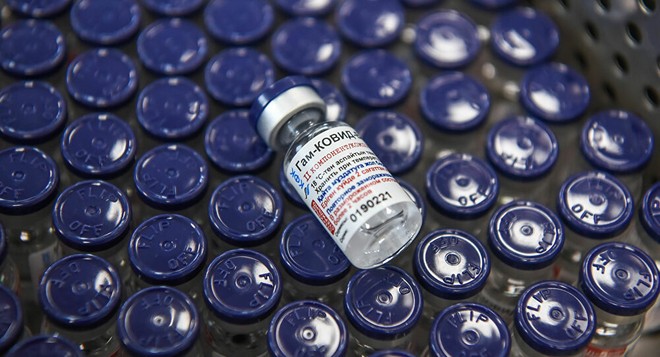
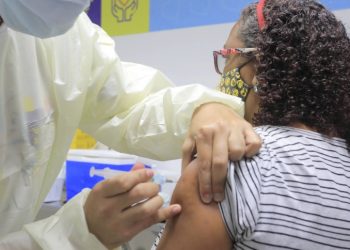
Nesta semana, a Agência Nacional de Vigilância Sanitária (Anvisa) vai deliberar sobre o pedido do Governo Federal sobre a importação da vacina indiana contra o coronavírus, a Covaxin. O órgão também analisará um pedido dos governadores para importação da vacina russa contra a Covid-19, a Sputnik V.
De acordo com a legislação aprovada pelo Congresso Nacional, a agência deveria ter apresentado um parecer final até hoje. No entanto, o ministro do Supremo Tribunal Federal (STF), Ricardo Lewandowski, aumentou em 5 dias o prazo para decisão.
Vale lembrar que a Anvisa já recusou a importação de ambas as vacinas. No caso da Covaxin, a agência apontou que a empresa Bharat Biotech, responsável pela produção do imunizante, falhou em apresentar documentação necessária, inclusive validação dos métodos farmacopeicos usados para fabricação.
Já a Sputnik V foi negada em meados de abril por apresentar riscos de segurança e falha na fabricação, segundo a agência reguladora. O Instituto Gamaleya ameaçou processar a Anvisa após essas acusações, alegando difamação por divulgação de informações falsas e imprecisas intencionalmente.
A Anvisa divulgou, em seguida, uma nota explicativa na qual afirmou estar negociando com o Fundo Russo o esclarecimento de algumas questões para finalmente liberar a importação do imunizante. Resta saber, ao longo desta semana, qual será o novo parecer da agência reguladora para as vacinas indiana e russa.
Embora uma das sócias da produtora da vacina Covaxin/BBV152 contra o coronavírus no Brasil esteja devendo R$ 20 milhões ao Ministério da Saúde, uma nova solicitação de autorização para importação de 20 milhões de doses do imunizante foi protocolada.
O Ministério da Saúde, em meados de março, já havia encaminhado requisição para importação e distribuição da Covaxin, uma vacina criada pela fabricante Bharat Biotech na Índia, onde tem autorização para uso emergencial. No entanto, a Agência Nacional de Vigilância Sanitária (Anvisa) negou o pedido após inspeção nas dependências da fábrica.
A Anvisa declarou que a Bharat Biotech falhou em apresentar certos documentos e especificações que devem ser estabelecidas para intermediários no processo. Além disso, não houve validação dos métodos farmacopeicos usados pela empresa. De modo geral, a fabricante não cumpriu os requisitos de Boas Práticas de Fabricação de Medicamentos exigidos pela agência.
Mesmo assim, o Governo Federal seguiu negociando tratativas com o órgão regulador para adequar os aspectos que motivaram a negativa.
Agora, o segundo pedido protocolado pelo Ministério da Saúde pode confirmar a liberação da importação do imunizante e dar continuidade ao Plano Nacional de Imunização (PNI) contra a Covid-19, que está atrasado. A perspectiva atual é que a vacinação de grupos prioritários seja finalizada somente em setembro.
Empresa que quer trazer a vacina indiana contra o novo coronavírus Covaxin ao Brasil, a Precisa Medicamentos tem entre suas sócias a Global Gestão em Saúde S.A.. Em reportagem da rádio BandNews FM, foi descoberto que a subsidiária deve R$ 20 milhões ao Ministério da Saúde.
A quantia se refere a compra de remédios de alto custo que nunca foram entregues aos pacientes de doenças raras. O contrato teria sido feito no final de 2017, durante a gestão do ex-ministro e atual líder do governo na Câmara, Ricardo Barros (Progressistas-PR).
Após mais de três anos do ocorrido, a pasta afirma ainda que o ressarcimento ainda está em negociação. Há uma ação do Ministério Público Federal em vigor contra a Global, Barros e servidores da época desde o fim de 2018.
Segundo a investigação, o atual líder do governo Jair Bolsonaro teria concedido benefícios à empresa nos contratos. Ao todo, o pedido no processo é que a companhia pague R$ 119,9 milhões em ressarcimento e danos morais a pacientes.
Produtora da Covaxin
A Precisa Medicamentos é parceira da farmacêutica indiana Bharat Biotech para a produção da vacina Covaxin no Brasil. O imunizante ainda não teve a Fase 3 do ensaio clínico concluída.
Apesar disso, o Ministério da Saúde negocia a compra de 20 milhões de doses com a empresa. O acordo já era para estar fechado, se não fossem “atrasos nos repasses de informações” pela empresa, e prevê entrega das doses no próximo mês de março.